Visualmente limpio: aportar claridad a las pautas regulatorias
Por Thomas Altmann, gerente técnico global de CIP/COP, Validación de Limpieza

Visualmente limpio es un término que se utiliza en casi todas las normas farmacéuticas (FDA, PIC/S, GMP). En pocas palabras, el equipo utilizado en la manufactura de productos farmacéuticos debe ser inspeccionado para determinar su limpieza visual antes del uso1.
Tiene mucho sentido; pero pocos tienen claro en un 100 % lo que significa visualmente limpio en los procedimientos operativos estándar y cómo documentarlo para una validación de limpieza. Las preguntas más frecuentes incluyen:
- ¿Cómo se ven los residuos?
- ¿Cuál es el umbral visual?
- ¿Cómo afecta la visibilidad el material de construcción?
- ¿Con qué frecuencia debe someterse a prueba la vista del inspector?
A continuación encontrará un breve desarrollo sobre cada uno de estos temas.
¿Cómo se ven los residuos?
Sus inspectores tienen que saber qué están buscando cuando inspeccionan los equipos. Deben poder diferenciar entre los residuos del proceso y los residuos que dejan los detergentes y productos desinfectantes, y cómo aparecerían los bajos niveles de cada tipo de residuo. Además, los inspectores deben tener el conocimiento sobre cómo se ve una superficie visualmente limpia, como la coloración de los aceros, rasguños u otros daños que no afectan el siguiente paso en la producción.
Por ejemplo, los ingredientes farmacéuticos activos (API) con frecuencia aparecen en forma de polvo y los residuos de detergente pueden verse como manchas en la superficie.

Los API suelen aparecer en forma de polvo.

Los residuos de detergente suelen aparecer en forma de manchas.
Con frecuencia los inspectores que buscan la "limpieza visual" no ven los residuos de detergente. Los fabricantes farmacéuticos que usan detergentes diseñados para aplicaciones de alimentos y bebidas deben tener presente que los residuos de ingredientes no solubles en agua, como los inhibidores de corrosión o surfactantes específicos, podrían permanecer y crear una interacción inesperada con los residuos de los API y ser transportados al producto posteriormente fabricado.
¿Cómo afecta la apariencia el material de construcción?
Los residuos pueden verse diferentes dependiendo del material utilizado para construir el equipo a inspeccionar. Aproximadamente el 90 % de los equipos usados en los productos farmacéuticos está hecho de acero inoxidable, y el vidrio, el caucho y los polímeros como el teflón y EPDM representan la mayor parte del resto.
Al elegir equipos y capacitar inspectores, una de las cosas que se debe tener en cuenta es que descubrir residuos sobre superficies de polímero será más difícil que hacerlo en equipos hechos de acero inoxidable.
Con eso dicho, los equipos de acero inoxidable expuestos a altas temperaturas se decolorarán con el tiempo, y esto hará más difícil la identificación de residuos que cuando el equipo fue entregado. Las superficies de equipos con rasguños deberán volver a pulirse (si fuera posible) o ser reemplazadas, ya que la limpieza visual ya no podría verificarse con seguridad.

Los inspectores deben ser capacitados para darse cuenta cómo cada tipo de residuo aparece sobre cada tipo de superficie.

El aspecto del residuo puede verse afectado por los distintos acabados de los materiales (acero inoxidable en comparación con el teflón o acero inoxidable nuevo/pulido en comparación con su versión decolorada).
¿Cuál es el umbral visual?
El umbral visual es el nivel de concentración en el que un API o residuo se vuelve visible. Los fabricantes tienen que determinar el umbral visual para cada API o residuo, y luego compararlo con el nivel en el que ese API o residuo se vuelve toxicológicamente significativo. Si el umbral visual es menor que su nivel toxicológicamente significativo predeterminado para ese API o residuo de limpieza, entonces la limpieza visual es una medición válida.
El siguiente análisis muestra la concentración en la que el paracetamol (un API relativamente de bajo riesgo) se vuelve visible.
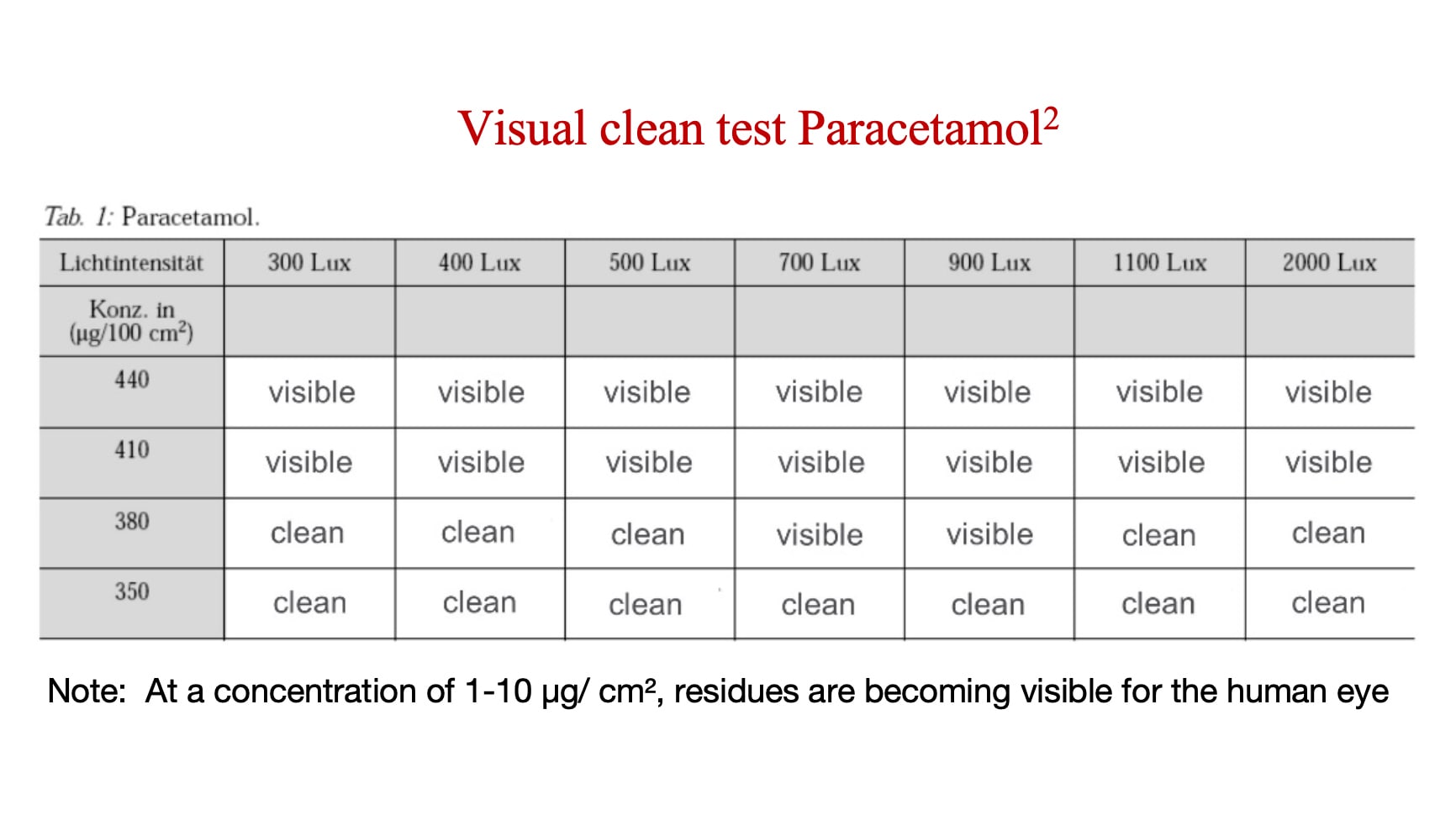
¿Con qué frecuencia debe someterse a prueba la vista del inspector?
Repito, las pautas no son específicas. Muchas compañías ahora requieren que todos los operadores que hacen inspecciones visuales se sometan a un examen de la vista todos los años.
Pero la ley no lo exige. Por otro lado, si sus procedimientos de limpieza son cuestionados, documentar que ha proporcionado una capacitación completa a sus inspectores y que les ha realizado exámenes de la vista con regularidad será muy útil para convencer a las agencias regulatorias que ha hecho todo lo que podría esperarse razonablemente.
¿Tiene más preguntas?
Para obtener más información sobre las buenas prácticas y las pautas de limpieza visual, comuníquese con Ciencias de la Vida de Ecolab. Estamos presentes en establecimientos farmacéuticos de todo el mundo y podemos ofrecer una perspectiva sobre cómo otros fabricantes han implementado la limpieza visual en sus programas de validación de limpieza.
1La norma 21 CFR Parte 211.67 de la FDA exigió en el punto (6) la inspección de equipos para determinar su limpieza inmediatamente antes de su uso
2Pharm. Ind. 62, N.° 6 (2000) Buscalferri y otros - Reinigungsvalidierung


